
 日期:2026/3/27
日期:2026/3/27 来源:
来源:
2026年3月20日,合肥综合性国家科学中心大健康研究院崔国梁和吴晶霞研究团队,与德国图宾根大学Alaa Madi博士、南京医科大学王曦课题组合作,在期刊《Nature Metabolism》发表题为“DGAT1 mediates sex-specific CD8+ T cell antitumour responses”的研究文章。该研究发现一个名为DGAT1(二酰甘油酰基转移酶1)的代谢酶可通过在雄性小鼠中解毒雄激素受体(AR)信号,进而抑制内质网应激介导的细胞死亡并维持 T 细胞干性;揭示了肿瘤微环境中存在性别特异性的代谢适应模式这项研究不仅从代谢维度揭示了肿瘤免疫的性别差异,更开辟了性别特异性免疫治疗的新方向。
首先通过分析公共数据库和自主测序数据发现,无论是人类肿瘤浸润CD8+ T细胞还是小鼠肿瘤模型中的CD8+ T细胞,DGAT1的表达水平均显著上调,且其表达谱与PD1、Rgs16等经典耗竭标志物高度吻合。这一发现提示DGAT1可能参与了CD8+ T细胞在肿瘤微环境中的功能调控。
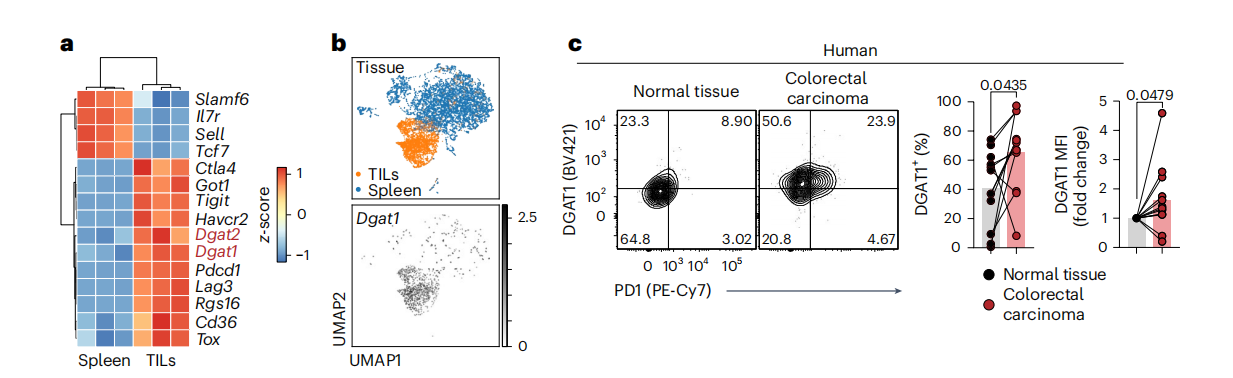
图1. DGAT1在小鼠和人类肿瘤浸润性CD8+ T细胞中上调。
为了探究DGAT1在CD8+ T细胞抗肿瘤免疫中的具体功能,研究团队构建了T细胞特异性敲除Dgat1基因小鼠,并对小鼠皮下荷瘤构建小鼠肿瘤模型,如黑色素瘤和结直肠癌模型。当研究人员按性别对数据进行分层分析后,一个鲜明的性别二态性显现出来:雌性Dgat1敲除小鼠中,肿瘤生长得到明显控制小鼠的生存期延长;雄性Dgat1敲除小鼠中,同样的基因敲除却导致肿瘤生长加速小鼠的生存期显著缩短。这一现象在两种不同的肿瘤模型中均得到验证,且通过流式细胞术分析发现,对比野生型雌鼠和雄鼠,雌鼠TILs中CD8+ T细胞的密度(T细胞数量/肿瘤重量)显著高于雄鼠;对比T细胞Dgat1缺失的小鼠和野生型,把T细胞中的Dgat1敲除掉之后,雌鼠TILs中CD8+ T细胞的密度没有显著变化,Slamf6+ Tim3-耗竭前体细胞的比例增多;雄鼠CD8+ T细胞的密度有显著上升,耗竭前体细胞的比例显著减少。
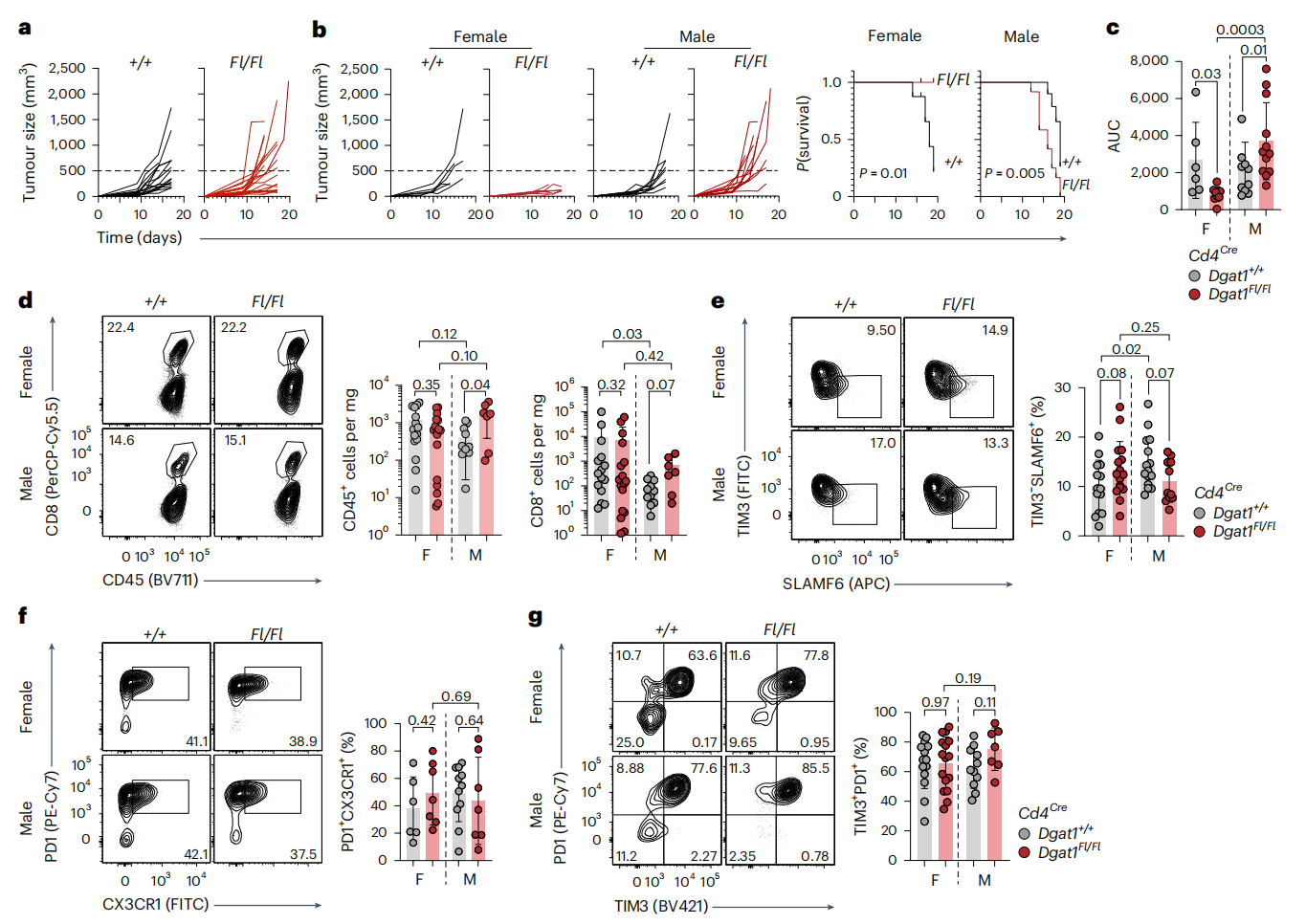
图2. DGAT1在肿瘤浸润T细胞中的性别二态性功能。
为什么同一个代谢酶在性别间会有如此差异?为了寻找问题的答案,研究团队通过将CD4-cre Dgat1 flox/flox小鼠和P14小鼠杂交,获得P14 CD4-cre Dgat1 flox/flox小鼠和其野生型对照P14小鼠。P14小鼠是一种转基因小鼠,其中含有大量可以识别LCMV病毒GP33-41表位的P14 T细胞。采用过继转移实验,将野生型和Dgat1敲除的P14T细胞分别转入预荷B16- GP33肿瘤的雌雄小鼠体内,结果发现:Dgat1敲除的T细胞在雌性受体小鼠内的抗肿瘤能力、TIM3- SLAMF6+耗竭前体细胞比例和供体细胞数目显著高于雄性受体小鼠。这一结果表明,决定T细胞命运的并非细胞自身的基因型,而是其所处的微环境。
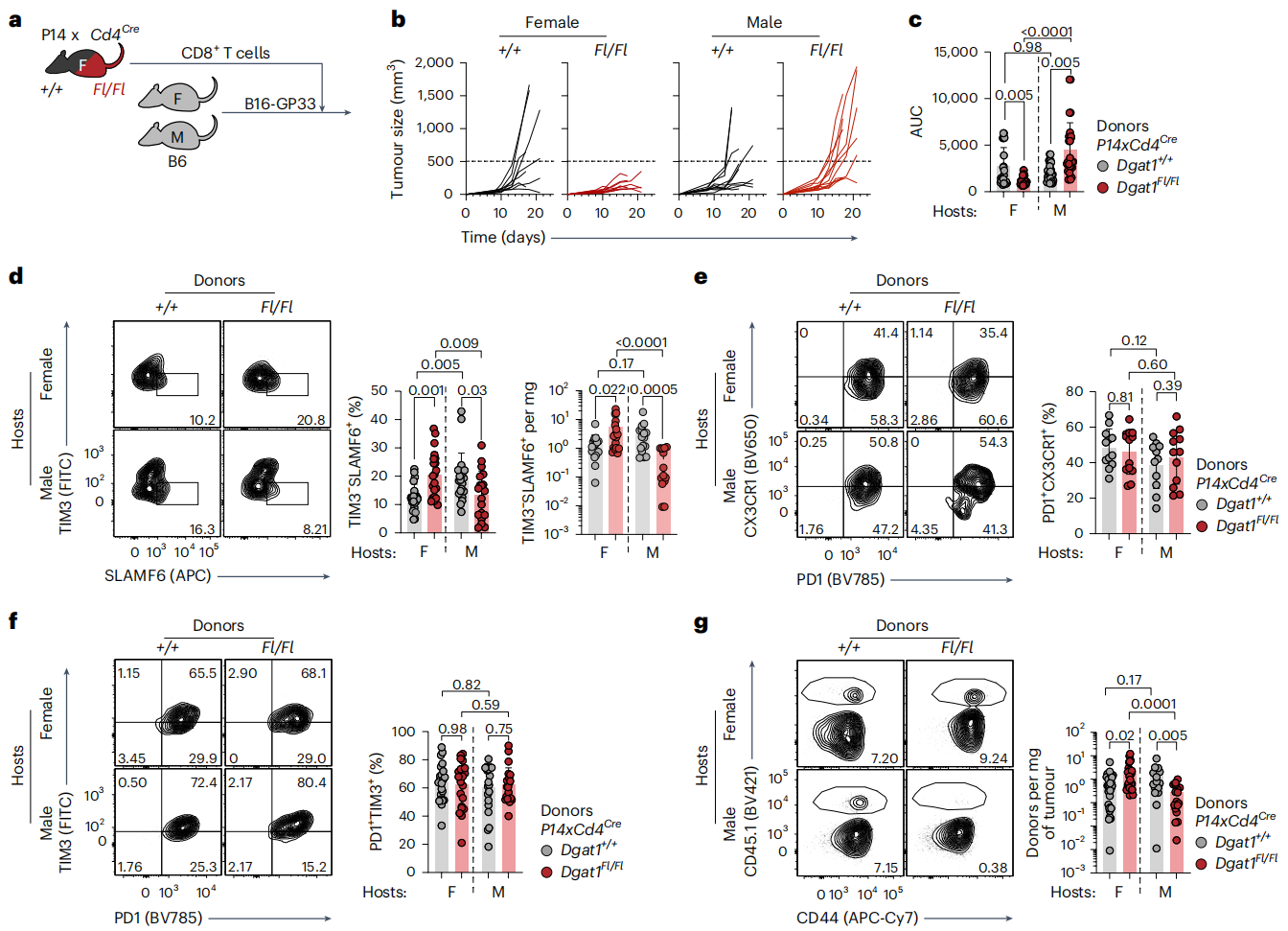
图3. DGAT1的性别二态性功能是CD8+T细胞内在且依赖于微环境因素。
深入机制研究发现,雄激素受体(AR)信号与Dgat1缺失共同作用,调控了耗竭T细胞的脂质过氧化水平、线粒体形态和内质网应激水平。
通过代谢组学和生物信息学分析,研究团队发现雌性和雄性小鼠肿瘤微环境中甘油磷脂、脂肪酸、甘油一酯、甘油二酯和甘油三酯等代谢物的组成和水平有显著差异。
通过流式细胞技术和透射电镜观察,研究团队发现耗竭T细胞中活性氧水平和过氧化脂质的含量随着睾酮浓度的增加而升高,Dgat1的缺失加剧细胞内脂质的过氧化。
Dgat1的缺失使耗竭T细胞内线粒体的数量增多;T细胞内质网肿胀减轻;睾酮处理过的Dgat1缺失型耗竭T细胞线粒体的长度缩短,“洋葱样”的同心圆结构增多,内质网肿胀加剧,呈内质网应激状态。
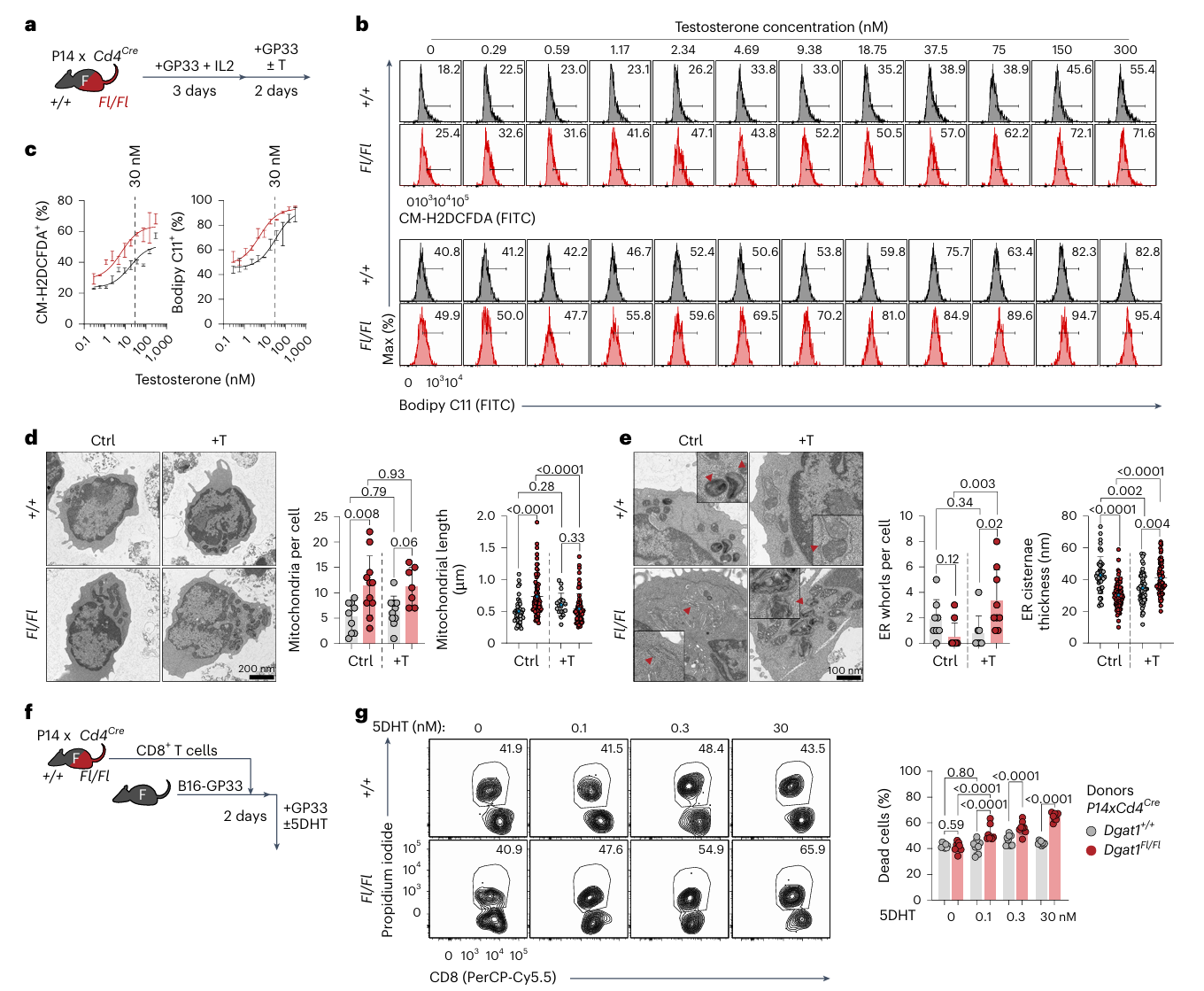
图4:在慢性活化的 Dgat1 敲除 CD8+ T 细胞中,雄激素受体(AR)信号可诱导脂质过氧化及细胞死亡。
为了进一步验证这一机制,研究团队检测了抑制细胞铁死亡或内质网应激诱导的死亡是否可以回复Dgat1敲除引起的表型。
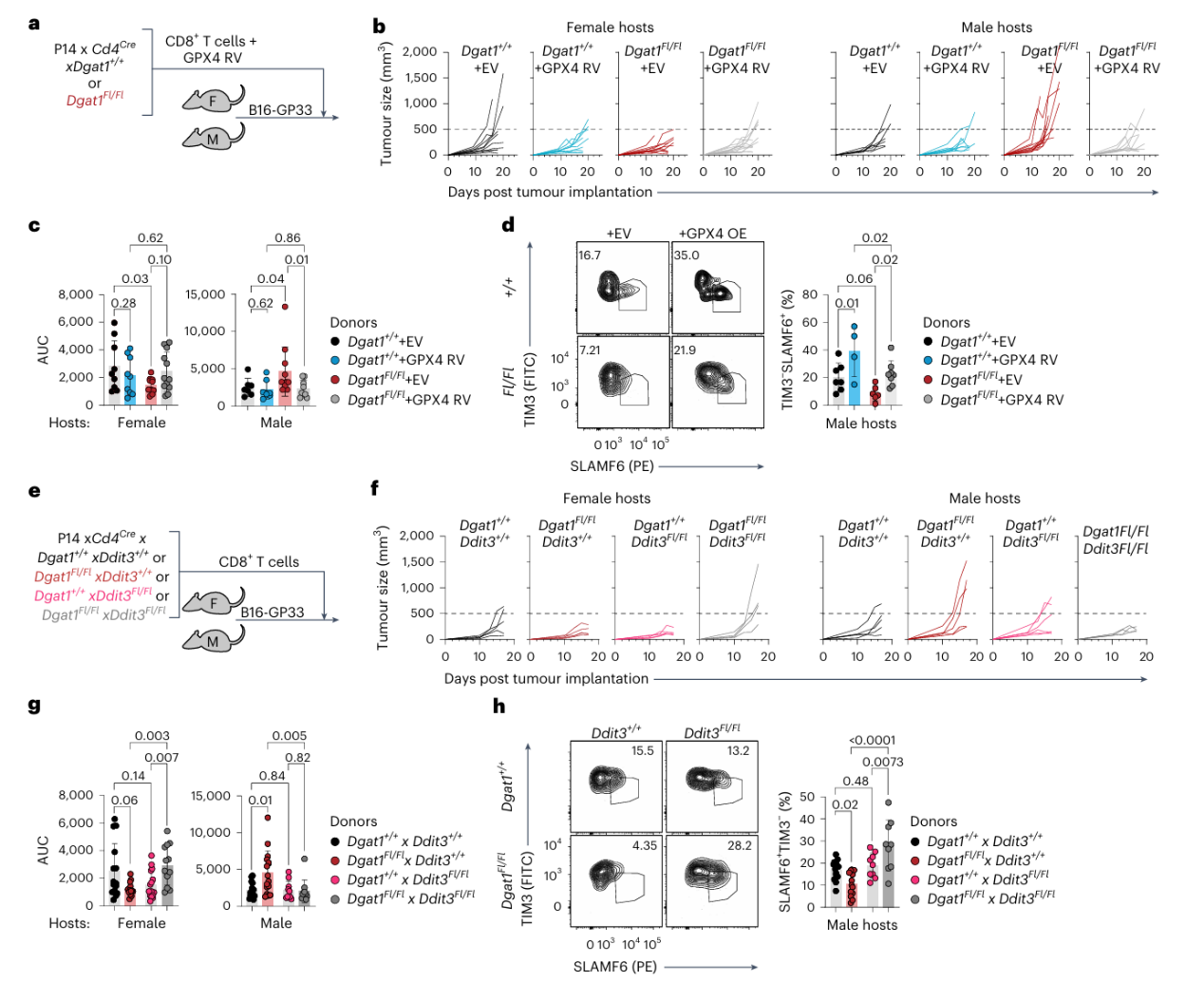
GPX4(谷胱甘肽过氧化物酶4)是细胞清除过氧化脂质的关键酶。研究团队通过逆转录病毒将GPX4或空载体导入Dgat1敲除的P14 细胞或野生型对照P14细胞,然后将这些细胞分别过继转输到预荷瘤雌性和雄性小鼠体内。结果显示,在雄性荷瘤小鼠中,过表达GPX4的Dgat1敲除T细胞抗肿瘤能力显著高于过表达空载体的Dgat1敲除T细胞,肿瘤生长得到有效控制,Slamf6+ Tim3-耗竭前体细胞比例显著升高。
DDIT3是内质网应激诱导凋亡的关键因子。研究团队构建了T细胞特异性敲除Ddit3的小鼠,将它和T细胞特异性敲除Dgat1的小鼠杂交,获得了野生型对照、T细胞特异性单敲Ddit3、T细胞特异性单敲Dgat1和T细胞特异性Dgat1和Ddit3双敲P14小鼠,然后将四种小鼠的P14细胞分别转输到预荷瘤雌性和雄性荷瘤小鼠体内。结果显示:在雄性受体鼠体内,Dgat1和Ddit3双敲除的P14细胞抗肿瘤能力和Slamf6+ Tim3-耗竭前体细胞的比例显著高于Dgat1单敲除的P14细胞。
上述实验证明DGAT1 对于抑制雄激素受体(AR)信号下游脂质过氧化所介导的内质网应激具有不可或缺的作用。
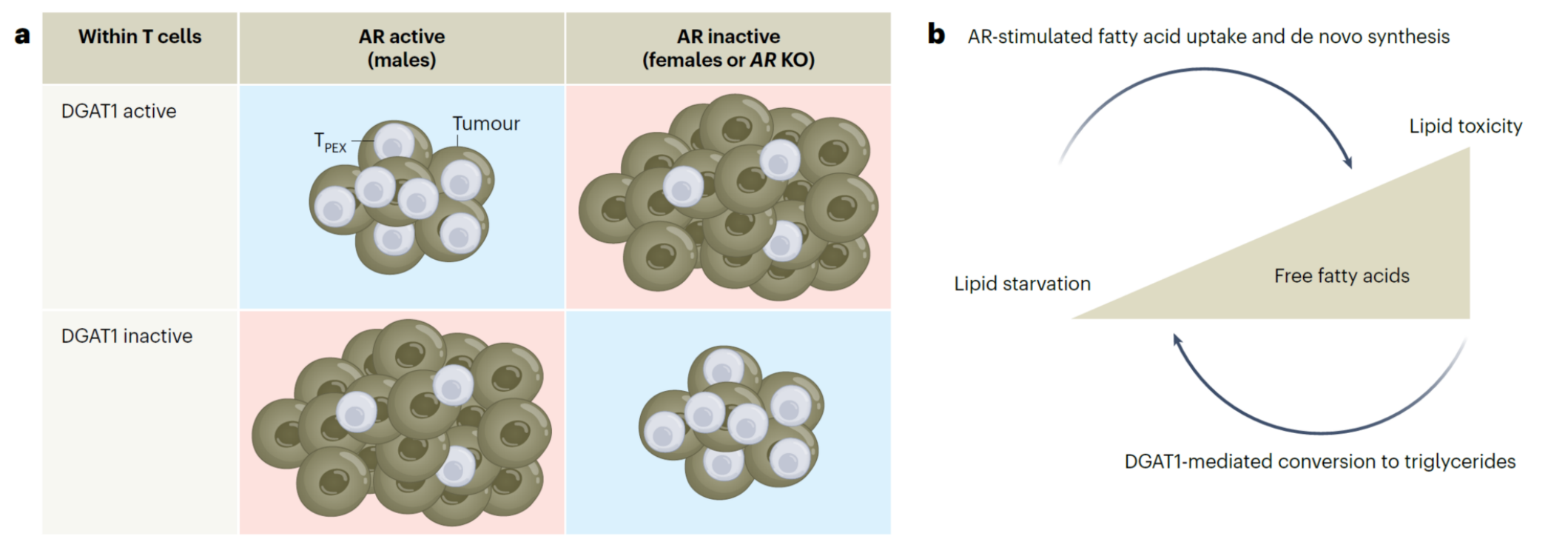
综上所述,该研究证实 DGAT1 以性别二态性方式调控抗肿瘤 CD8+T 细胞功能。DGAT1 在雌性小鼠中对耗竭前体 T 细胞(progenitor Tex 细胞)具有不利作用,而在雄性小鼠中则为其必需因子。联合雄激素受体(AR)信号分析发现,DGAT1 缺失可导致脂质过氧化物蓄积、内质网应激及细胞死亡。抑制 DGAT1 功能或可成为潜在的肿瘤免疫治疗策略,但该策略仅适用于不存在协同 AR 信号活化的情境。约翰斯?霍普金斯大学西德尼?金梅尔综合癌症中心的Laura A. Sena教授在同一期的Nature Metabolism杂志对这一工作做出了名为“Fat chance of male and female equality in tumour immunity”的专题评论,指出这项研究具有开创性意义,并赞赏将性别作为生物学变量加以考量。
研究论文文章链接:https://doi.org/10.1038/s42255-026-01462-7
评论文章链接:https://doi.org/10.1038/s42255-026-01469-0